Service Center
在精密的实验室里,纯水和超纯水扮演着至关重要的角色,在实验的过程中,它们是确保数据准确无误的关键,也是实验操作的基石。但实验员们常会遇到两个问题:“纯水pH测得值偏酸”以及“超纯水pH测得值不稳定”。这让一些实验员们产生了疑惑,数值的变化是否会对实验结果产生影响?别担心,这些都是正常现象,下面我们就来揭开它们的秘密,并分享一些实用的解决方法。
一、纯水pH值偏酸
纯水与环境之间的微妙互动,尤其是与空气中的二氧化碳,构成了其pH值偏酸性的关键。
当纯化水机进行反渗透过滤时,由于CO2分子与水分子的尺寸相近,使得RO膜难以将已溶解在原水中的CO2完全除去。同时,对于已经制备完成,并储存在纯水箱(罐)中的纯水,在储存、备用的过程中也会不可避免地与空气接触,使CO2溶解在纯水中。这些溶解做纯水中的CO2与水分子发生反应,产生碳酸,导致纯水的pH值偏酸。
对纯水箱(罐)中的纯水pH值持续性地监测会发现,暴露在空气中的纯水pH值从7降至5.7仅需一天,而在两天的时间内将会继续降低至4.7。
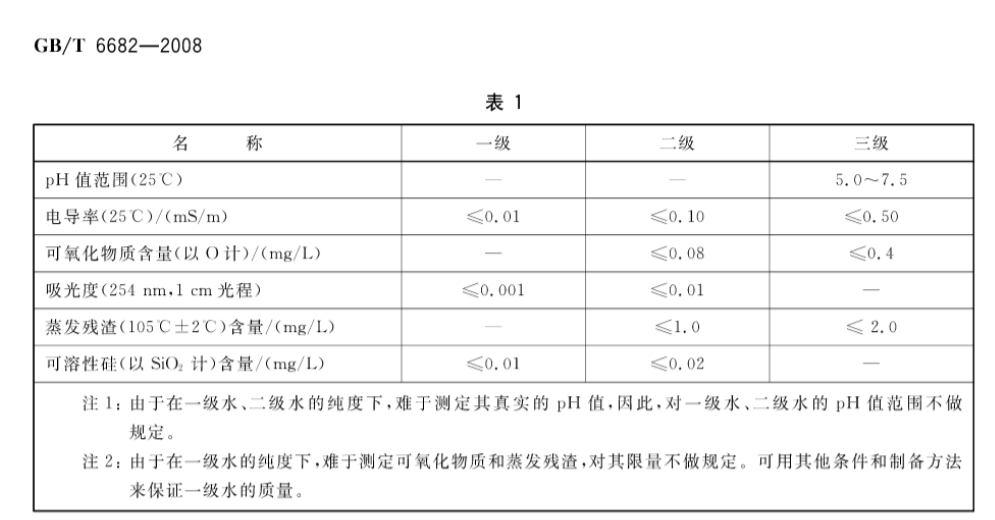
这一变化清晰地展示了纯水对空气中二氧化碳的敏感性,也是GB/T 6682-2008《分析实验室用水规格和试验方法》为三级水设定5.0-7.5 pH值范围的科学依据。
二、超纯水pH值不稳定
超纯水通过复杂的纯化技术流程,几乎去除了所有杂质,达到了电阻率18 MΩ·cm以上的高标准。然而,这份极致的纯净也带来了pH值检测的不稳定性。
pH仪器的检测原理是通过水中含有的离子在电极的作用下定向移动而形成电路,最终显示读数。超纯水中的离子含量极低,缓冲的能力弱,因此一个细微的外界影响都会引起pH值的波动。而在现实情况中,只要超纯水与空气接触,空气中的CO2将会溶解到水中,产生碳酸。同时,由于超纯水中缺乏自然的缓冲体系CO2的溶解必将会引起超纯水pH值的波动。
国家标准GB/T 6682-2008明确指出,一级水和二级水由于纯度过高,难以准确测定真实的pH值,因此未对其pH值范围做出规定。
三、解决方案
1、纯水的密封保存
无论是纯水还是超纯水,引起pH值变化的主要原因之一便是空气中的CO2,而市面上绝大部分的纯化水设备储存纯水的容器为水箱或水罐,纯水在水箱(罐)内储存备用的过程中,其不可避免地会与空气中的CO2接触,就必将导致纯水pH值的波动。因此,若能采用隔绝空气的储存方式,就可以在极大程度上规避不必要的偏差。
2、超纯水的即取即用
超纯水中溶解的离子浓度极低,除了可以溶解空气中的二氧化碳,形成碳酸以外,外界环境中还有,如颗粒,挥发性有机物、细菌及其他污染物等,都会进一步使水质衰退。因此,超纯水需要即取即用,尽量避免因外界污染影响最终取用的超纯水水质。
除了以上两点原因,还有其他比如:是否定期检查设备运行状态、是否使用了符合实验要求的取水容器,亦或者是否遵循标准的取水操作流程,都是会对纯化水或超纯水pH值产生影响的因素。只有我们把握好每一个环节,才能在最大程度上降低pH值波动对实验结果带来的影响。
通过深入理解纯水与超纯水pH值变化的科学原理,实验人员可以更加精准地控制实验条件,提高实验的准确性和可靠性。实验室纯水和超纯水的pH值奥秘,不仅是一次科学之旅,也是实验成功的关键。
扫一扫在手机打开当前页